En god förlossningsvård syftar till att ge det nyfödda barnet en god start på livet och de blivande föräldrarna en positiv upplevelse, samtidigt som förlossningen ska vara medicinskt säker. De allra flesta barn föds friska och utan tecken på påverkan av förlossningen.
Fostrets tillstånd före förlossningen har stor betydelse för hur väl det kan klara av den stress som förlossningen innebär. Ett friskt och välnutrierat foster har välutvecklade skyddsmekanismer och klarar mycket stora påfrestningar utan att riskera att skadas.
De metoder som används för övervakning syftar till att följa fostrets utveckling (exempelvis symfys-fundus mätning och tillväxtultraljud) och att bedöma dess aktuella tillstånd (exempelvis CTG). Under förlossningen vill vi kontrollera och registrera hur viktiga vitala funktioner påverkas av den mekaniska och metaboliska stress fostret utsätts för på grund av värkarbetets påverkan på blodfödet till fostret.
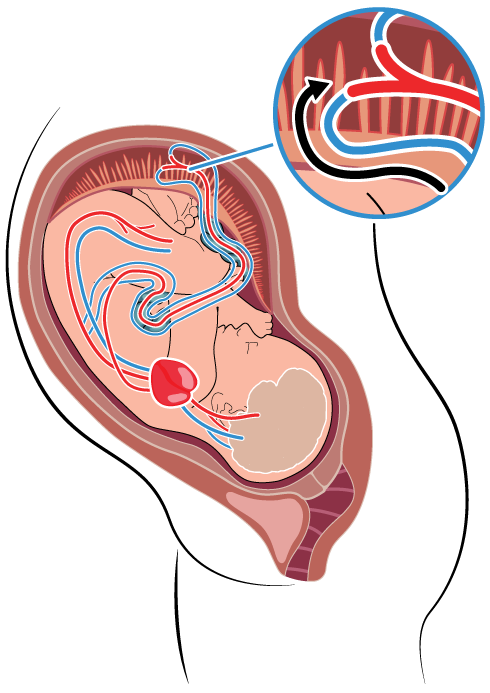
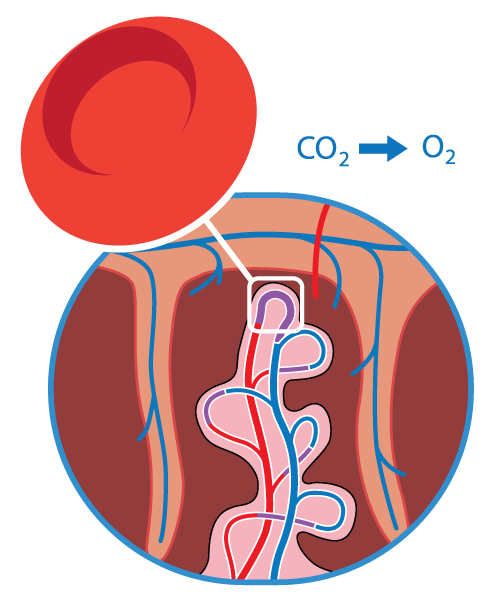
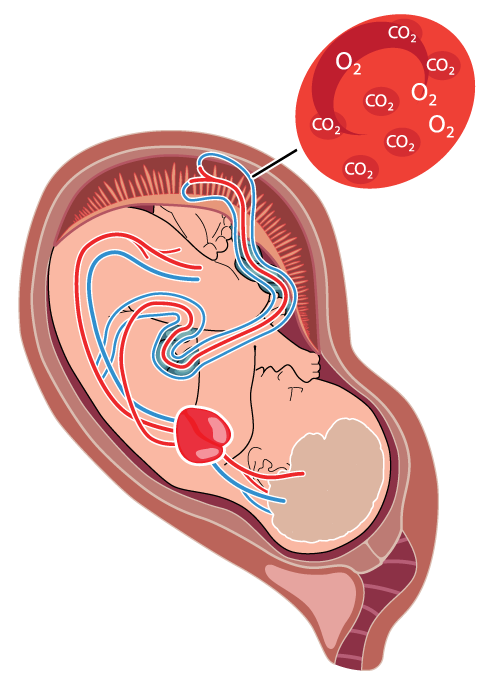
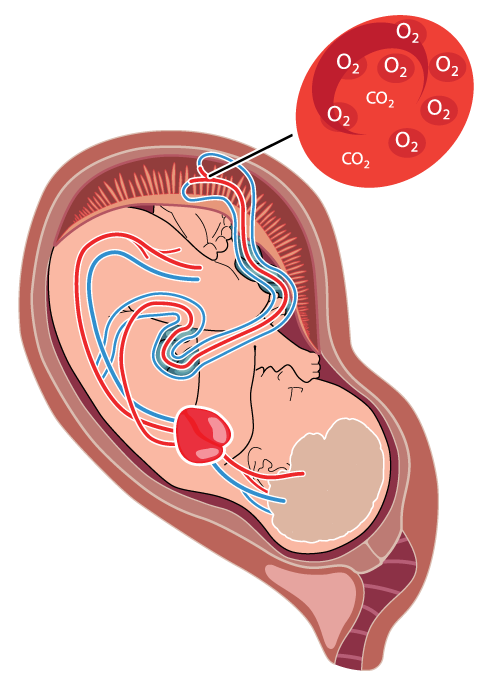
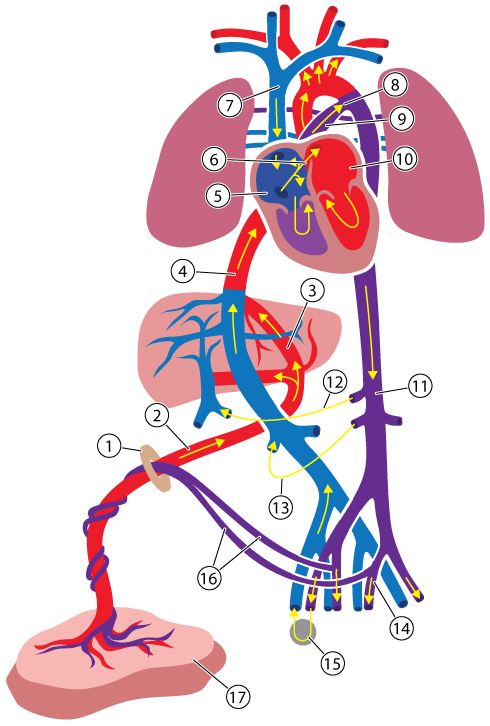
Mekanisk stress under förlossning betingas av att huvudet och/eller navelsträngen komprimeras när livmodern kontraheras. Metabol stress beror bland annat på att cirkulationen i moderkakans maternella del reduceras eller upphör vid varje värk när värkarbetet når en viss styrka. Gasutbytet mellan foster och mor kan då under perioder påverkas och syretillförseln försämras.
Om fostrets energireserver är begränsade, eller om påfrestningarna av värkarna är ovanligt stor, kan förmågan att kompensera för mekanisk eller metabol stess vara otillräcklig. Den kompenserade stressen övergår då i inkompenserad stress, vilket ibland betecknas fetal distress och innebär risk för syrebrist. Vitala funktioner kan då påverkas så allvarligt av syrebrist att barnet får varierande grader av fysiska och/eller mentala skador eller avlider.
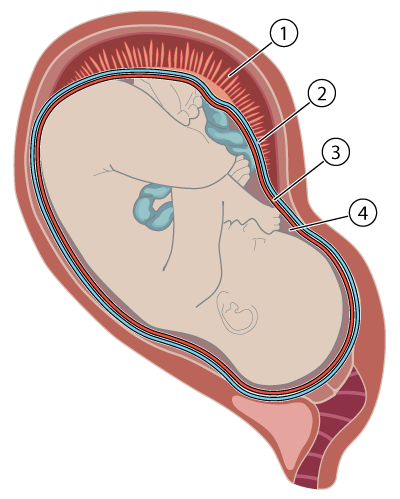
Om förlossningsförloppet avviker från det normala krävs åtgärder, grundade på kunskap om den gravida kvinnans och fostrets fysiologi. Detta kapitel beskriver de mekanismer fostret är beroende av för att klara sin födelse, och bakgrunden till hur fostret signalerar om syretillförseln påverkas.


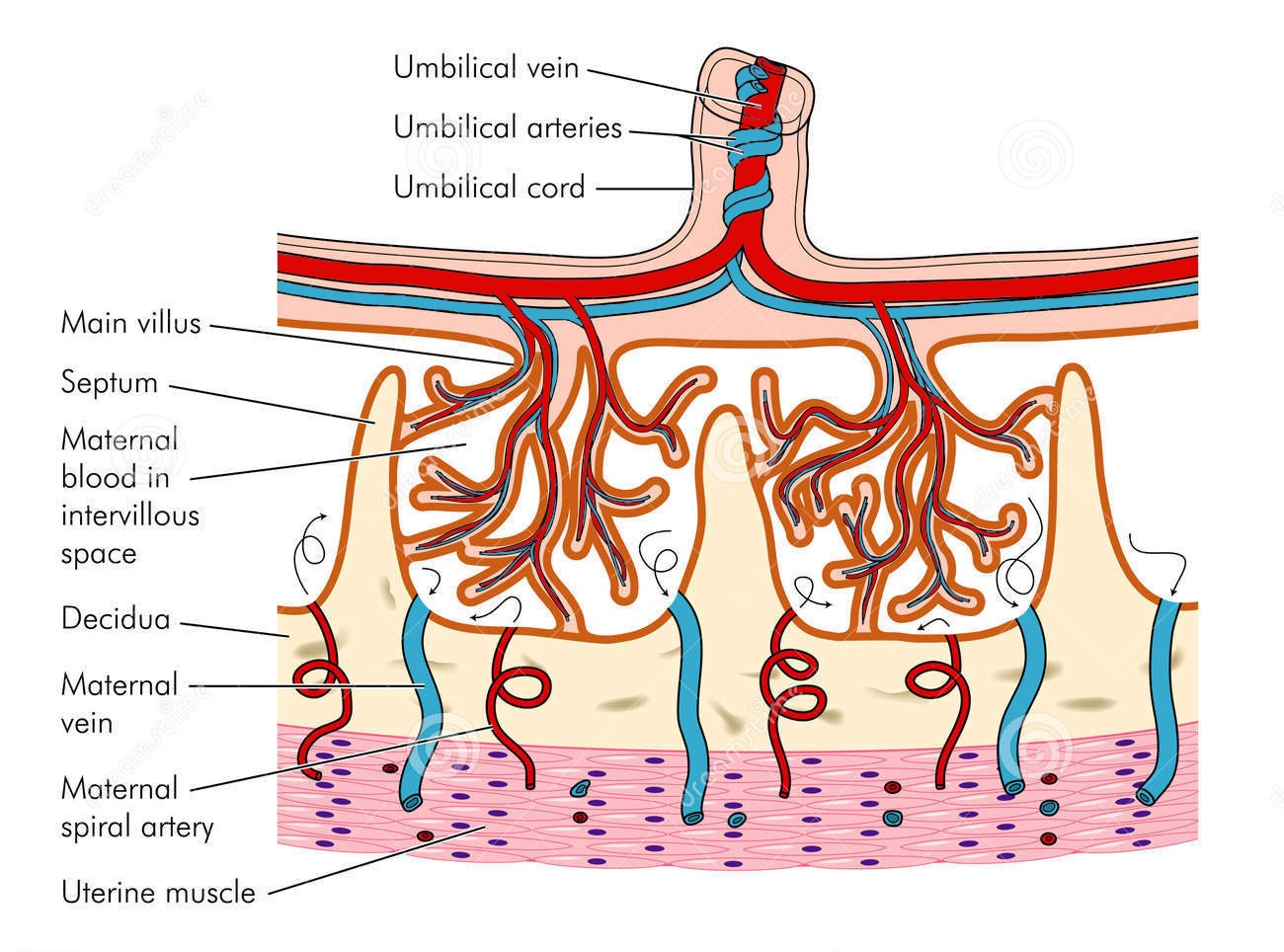
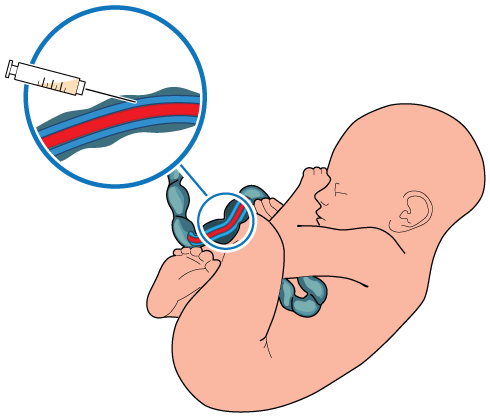
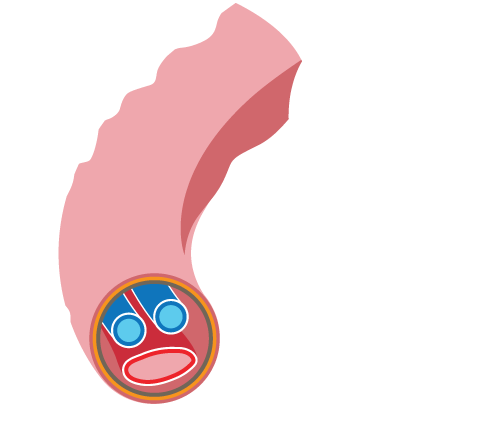 Navelsträng i genomskärning, två artärer och en ven
Navelsträng i genomskärning, två artärer och en ven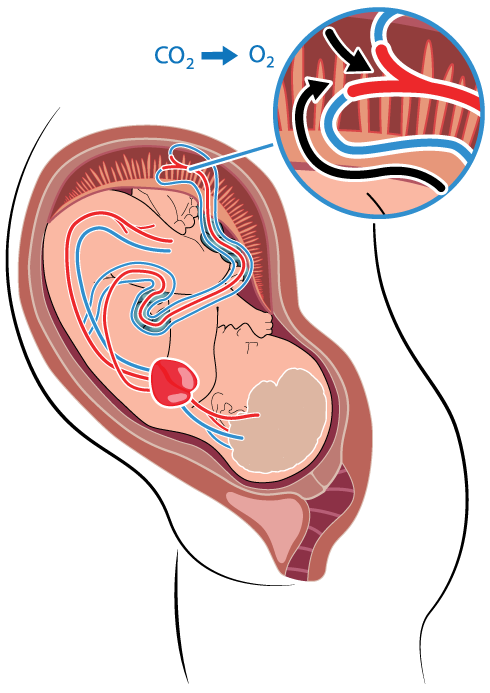
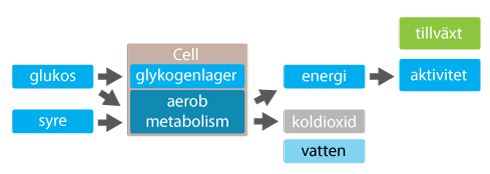
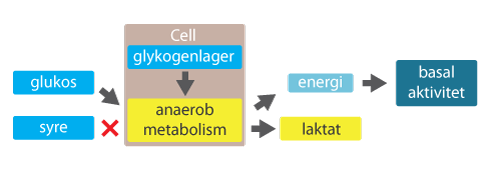
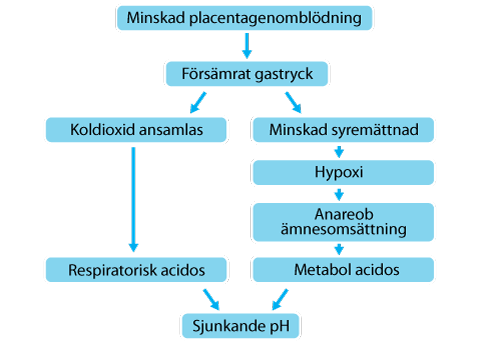 Utveckling av respiratorisk och metabolisk acidos
Utveckling av respiratorisk och metabolisk acidos
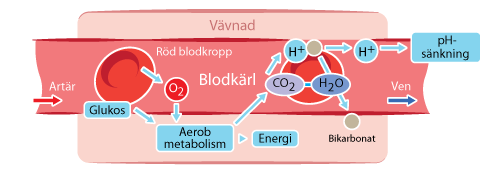 Respiratorisk acidos
Respiratorisk acidos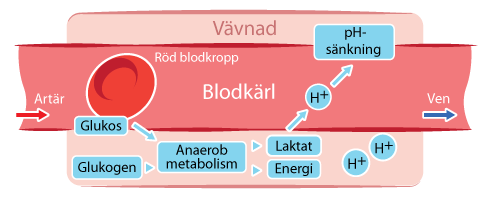 Metabolisk acidos
Metabolisk acidos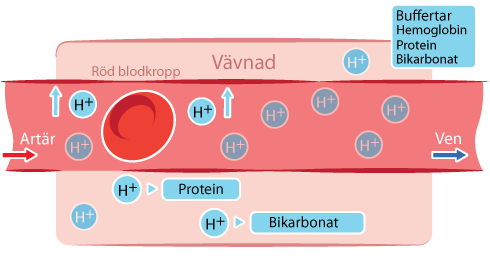 Kroppens buffertsystem
Kroppens buffertsystem
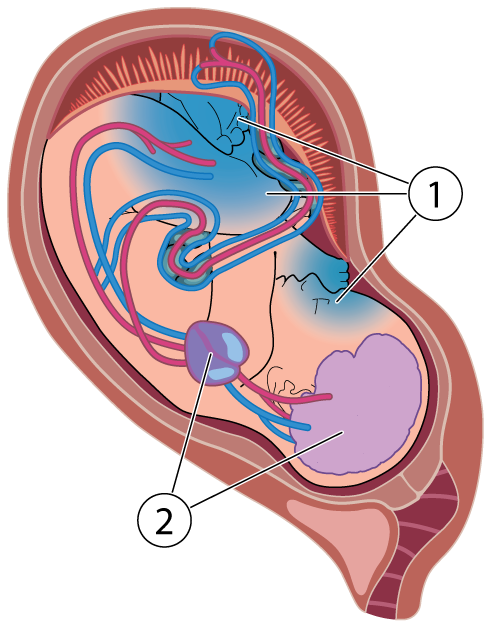
 Blodgasanalys
Blodgasanalys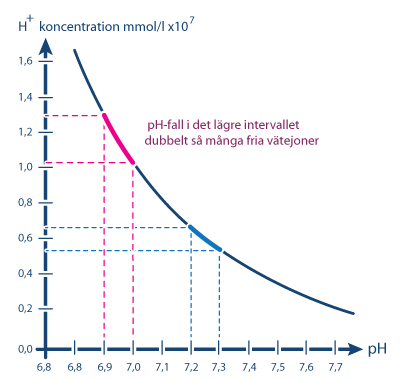 pH anger halten av fria vätejoner i blodet. Skalan för pH är logaritmisk; dvs det är en dubbelt så stor skillnad mellan pH 7,00 och 6,90 som mellan 7,30 och 7,20.
pH anger halten av fria vätejoner i blodet. Skalan för pH är logaritmisk; dvs det är en dubbelt så stor skillnad mellan pH 7,00 och 6,90 som mellan 7,30 och 7,20.
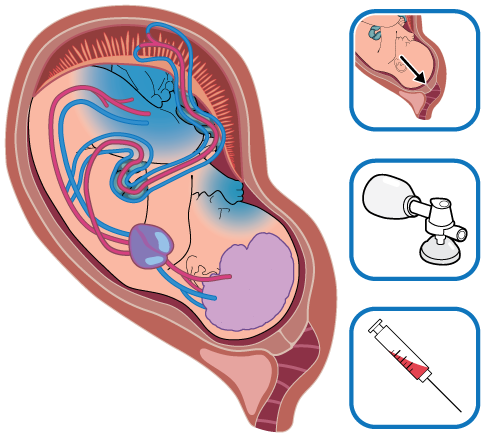 Bedömning av eventuell förlossningsskada
Bedömning av eventuell förlossningsskada